Tout savoir sur la néphrotoxicité médicamenteuse
Néphrotoxicité médicamenteuse : un problème médical fréquent
Le rein, organe majeur d’excrétion et richement vascularisé, est particulièrement vulnérable à la toxicité médicamenteuse (débit sanguin rénal =25% du débit cardiaque). Il possède la plus importante surface endothéliale.
La dissociation des liaisons protéiques se produit majoritairement au niveau rénal.
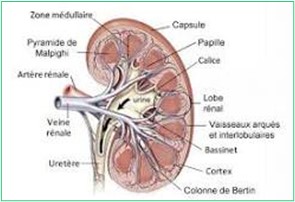
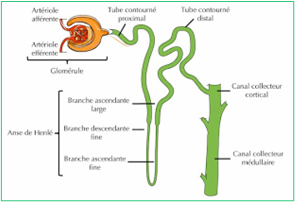
Le néphron constitue l’unité fonctionnelle du rein. La formation d’urine définitive passe par 3 étapes :
a. La filtration glomérulaire:
- Intéresse la fraction libre (non liée aux protéines/mécanisme passif), dépend de la fixation protéique des médicaments.
- Elle dépend de la taille des molécules (< 65000 Da) et du débit de filtration glomérulaire.
- Les médicaments filtrés sont présents dans la lumière tubulaire où ils se concentrent du fait de la réabsorption de l’eau.
- Les médicaments non filtrés se concentrent dans les artères efférentes et péritubulaires.
b. La sécrétion tubulaire
- C’est le passage des substances du sang des capillaires péritubulaires vers la lumière tubulaire au niveau du tubule contourné proximal (mécanisme actif).
- Compétition entre les médicaments éliminés par le même processus de transport actif, ce qui retarde l’excrétion de certains ions. Ce type d’interaction peut être exploité pour prolonger l’effet thérapeutique d’un médicament.
c. Réabsorption tubulaire:
- De la lumière tubulaire vers l’artériole péritubulaire,
- Peut être active (nécessitant transporteur et énergie) ou passive (concerne le plus souvent les substances liposolubles).
- Fonction rénale : désigne par convention le débit de filtration glomérulaire.
- Insuffisance rénale : diminution du débit de filtration glomérulaire.
- Insuffisance rénale aiguë : désigne un état dans lequel la filtration glomérulaire décline rapidement (quelques minutes à quelques jours) et de façon continue.
Les causes de la diminution de la filtration glomérulaire et de l’IRA peuvent être :
- Pré-rénales fonctionnelles : par hypovolémie, état de choc, insuffisance cardiaque, sepsis. Le parenchyme est intact. Dans un premier temps, la vasoconstriction de l’artère efférente maintient un DFG normal, puis la pression de filtration baisse et l’IRA apparaît..
- Parenchymateuses : par lésions des différentes structures du rein (nécrose tubulaire aiguë ischémique ou toxique), néphropathie interstitielle, glomérulopathie.
- Post-rénales : obstacle intra tubulaire ou sur la voie excrétrice.
1. Epidémiologie
Le développement des IRA est le plus souvent multifactoriel, cependant :
- 20% des patients admis pour IRA sont liés à une néphrotoxicité médicamenteuse.
- Elles peuvent représenter jusqu’à 66% des atteintes rénales aigües chez les sujets âgés.
- En pédiatrie, 16% des hospitalisations des IRA sont d’origine médicamenteuse.
- Environ 14% des IRA en réanimation sont d’origine médicamenteuse.
Les atteintes rénales aigües sont responsables :
- D’une augmentation de la mortalité.
- D’une augmentation des durées d’hospitalisation.
- D’une augmentation du coût de soins.
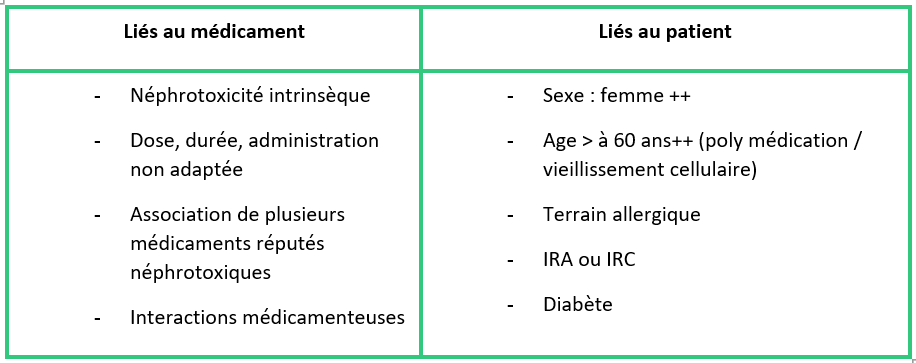
2. Facteurs de risques
Tous les patients exposés à des médicaments réputés comme néphrotoxiques ne développent pas d’insuffisance rénale.
Cependant, certains facteurs de risques peuvent rendre le rein plus fragile :
3. Mécanisme
La néphrotoxicité médicamenteuse se manifeste par divers mécanismes et peut potentiellement toucher toutes les parties du rein.
Il faut noter qu’un même médicament peut avoir à la fois :
- Plusieurs mécanismes toxiques.
- Une toxicité aigüe et chronique.
On distingue six types d’atteintes rénales induites par les médicaments :
- Les atteintes pré-rénales (hypoperfusion rénale)
- Les néphropathies tubulaires
- Les néphropathies interstitielles
- Les néphropathies glomérulaires
- Les néphropathies vasculaires (microangiopathie thrombotique)
- Les néphropathies obstructives (obstruction urinaire)
a. Les atteintes pré rénales (hypoperfusion rénale)
- IRA fonctionnelle.
- Le rein n’est pas suffisamment perfusé.
- Le sang arrive vers le rein avec une certaine pression (pression systolique) qui permet de pousser le sang à travers les membranes de filtration afin de former les urines.
- Certains médicaments vont modifier cette pression :
-
-
- AINS :
- Responsables de vasoconstriction de l’artère afférente à glomérule ne va pas filtrer correctement à IRA.
- Diurétiques :
- Responsable d’une augmentation de la diurèse à déshydratation à hypoperfusion rénale à IRA.
- IEC/ ARAII :
- Ce sont des médicaments antihypertenseurs et néphroprotecteurs.
- Responsables d’une vasodilatation de l’artère efférente, si cette vasodilatation est très importante par rapport à l’artère afférente donc une accélération de la circulation au niveau du glomérule à passage très rapide du sang à pas assez de temps pour une filtration glomérulaire efficace à IRA (à juste dose ils sont néphroprotecteur/ à dose élevée ou longue durée ils peuvent devenir néphrotoxique).
- AINS :
-
b. Les néphropathies tubulaires
On distingue deux types qui sont responsable d’une IRA :
- Toxicité directe :
- Le médicament agresse directement les cellules tubulaires (principalement les Aminosides et les produits de contraste iodés).
- Toxicité indirecte :
- Ce n’est pas le médicament en lui-même qui est toxique mais ses effets secondaires :
Statines : indiqués en cas hypercholestérolémie à Rhabdomyolyse à libération de la myoglobine toxique pour la cellule tubulaire.
Acyclovir : un antivirale à Hémolyse à libération de la bilirubine toxique pour la cellule tubulaire.
c. Les néphropathies interstitielles
- IRA par inflammation de l’interstitium rénale et des tubules avec œdème ou fibrose.
- Mécanisme immunologique où le médicament devient antigénique en se fixant sur la basale du tubule ou de l’interstitium (Allergie rénale).
-
-
- AINS
- B-Lactamines
- Allopurinol
-
d. Les néphropathies glomérulaires
On peut avoir :
- Lésions glomérulaires minimes : Ex : AINS.
- Glomérulo-néphrite extra membraneuse : Ex : Sel d’or.
e. Les néphropathies vasculaires (microangiopathie thrombotique)
- Lésion de l’endothélium des artérioles et des capillaires entraînant la formation d’agrégats plaquettaires et de thromboses.
- Les anticancéreux : Mitomycine, Bléomycine, Gemcitabine, Cisplatine
- Les immunosuppresseurs : OKT3, Cyclosporine, Tacrolimus,
- Les antiagrégants plaquettaires : Ticlopidine, Clopidogrel
f. Les néphropathies obstructives (obstruction urinaire)
- Responsable d’une IRA obstructive.
- On distingue deux mécanismes :
-
-
- Cristallurie : le médicament constitue le noyau pour développer une lithiase. Exemple : Acyclovir.
- Fibrose rétro-péritonéale : engainant les uretères. Elle est moins évidente le matin à cause de la sécrétion maximale de cortisol, et devient plus symptomatique avec sa diminution. Exemple : Bêta-lactamine.
-
4. Diagnostic
Le diagnostic de l’IRA se fait essentiellement sur une évaluation du débit de filtration glomérulaire.
a. Cliniquement
Le débit urinaire est le seul reflet direct de l’excrétion rénale.
b. Biologiquement
- Urée plasmatique.
-
-
- Entièrement filtrée par les glomérules.
- Son taux sanguin reflète le fonctionnement global des reins.
- Sa concentration plasmatique est notablement influencée par certains facteurs extra rénaux : teneur en protéines de l’apport alimentaire, fièvre, diurèse.
-
- Créatinine plasmatique
-
-
- Eliminée uniquement par les reins.
- Le taux sanguin est un meilleur marqueur de la fonction rénale.
-
- Clairance de la créatinine
-
-
- Etant éliminée par filtration glomérulaire ; la mesure de la clairance de la créatinine permet d’évaluer le débit de filtration glomérulaire.
-
- Biomarqueurs du futur :
-
-
- Cystatine C; NGAL……
-
- DFG d’un glomérule = volume de plasma passant à travers la paroi capillaire glomérulaire par unité de temps.
- DFG = somme des DFG de tous les glomérules
Principales formules d’estimation du DFG dérivées de la créatinine et/ou de la cystatine :

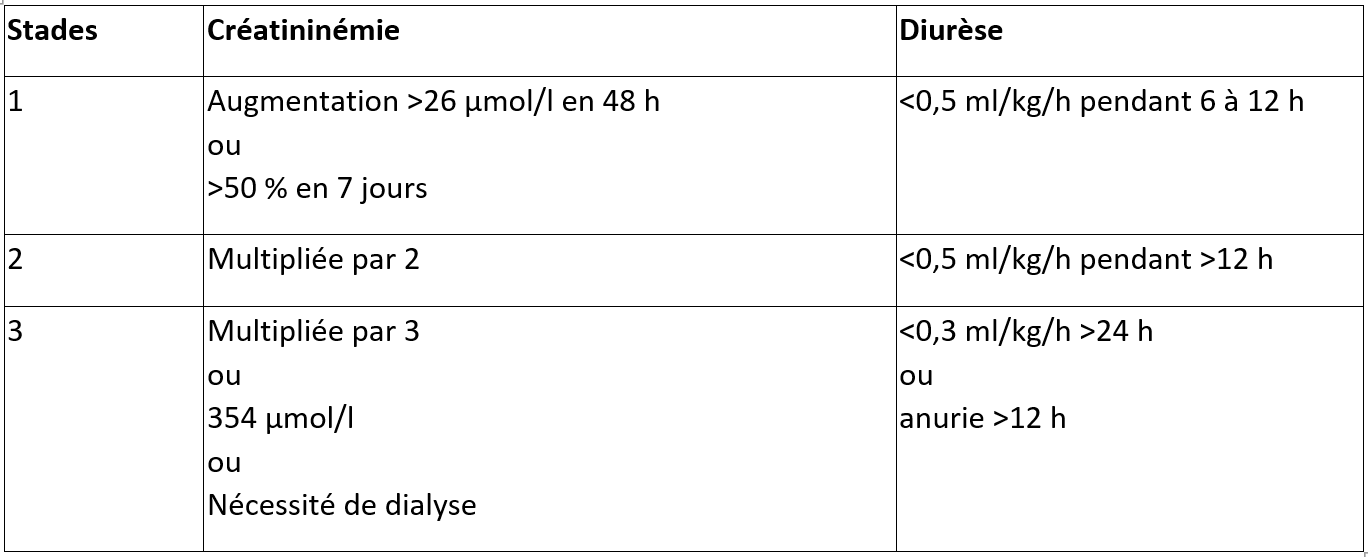
Stades de l’insuffisance rénale aiguë
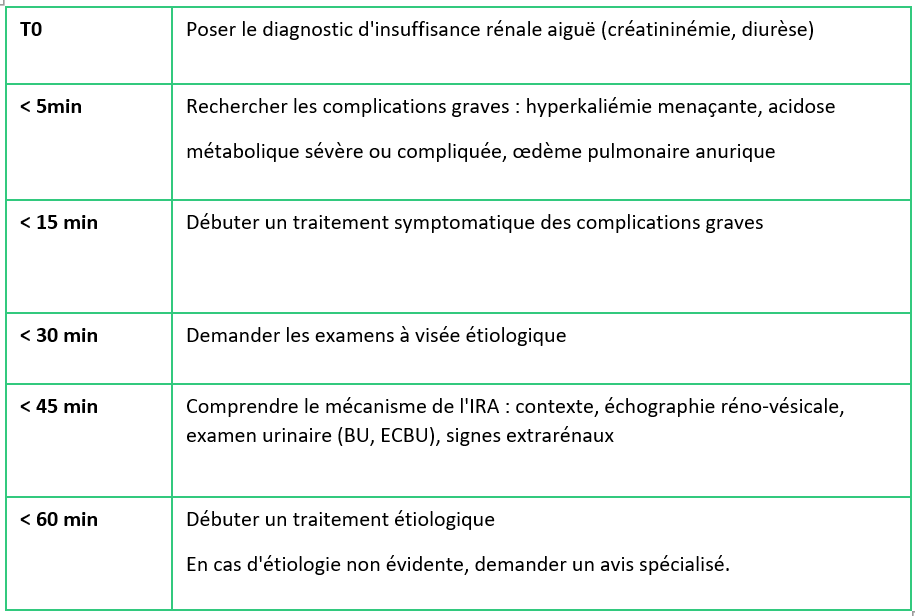
5. Prise en charge
Par défaut, il faut considérer une insuffisance rénale comme aiguë.
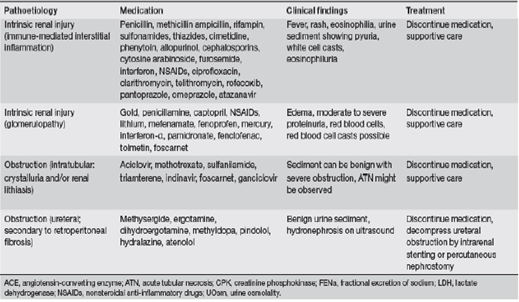
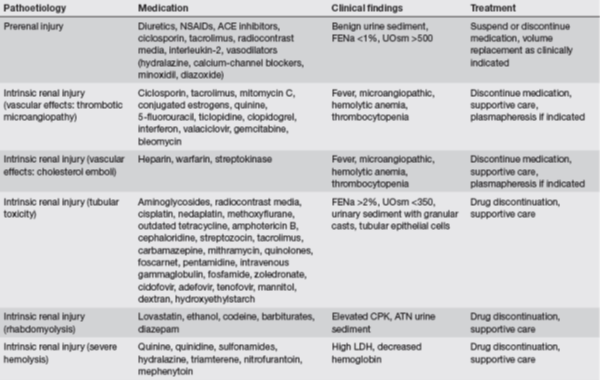
D’après D. Choudhury and Z. Ahmed, Drug-associated renal dysfunction and injury, Nat Clin Pract Nephrol. févr, vol.2, issue.2, pp.80-91, 2006, les différents mécanismes de la néphrotoxicité ont été classés dans le tableaux suivant en fonction des médicaments responsables, la symptomatologie (clinique ou biologique) et la prise en charge :
6. Conclusion
- Aucune molécule n’a pour l’instant démontré son efficacité pour la prévention de la néphrotoxicité médicamenteuse.
- Lutter contre l’automédication et le prescription intempestive et erronée des médicaments.
- Identification des facteurs de risque afin d’évaluer la balance bénéfice/risque (La connaissance des facteurs de risque et des mécanismes de néphrotoxicité sont la base d’une meilleure prévention et également d’une meilleure prise en charge).