Focus métier – MedDRA Dictionary
MedDRA, c’est quoi ?
La terminologie du Dictionnaire Médical des Affaires Réglementaires (Medical Dictionary for Regulatory Activities : MedDRA), est la terminologie médicale internationale développée à l’initiative du Conseil International d’Harmonisation des exigences techniques. Cela, pour l’enregistrement des médicaments à usage humain (ICH) et la MSSO (Organisation des services d’assistance et de maintenance) qui est chargée par ICH de maintenir, développer et distribuer MedDRA.
Cette terminologie met l’accent sur l’utilisation pour la saisie, la récupération, l’analyse et l’affichage des données afin de fournir une classification approuvée au niveau international pour une communication efficace des données sur les effets indésirables entre les pays.
La terminologie MedDRA s’applique à toutes les phases de développement des produits médicaux à usage humain, à l’exclusion de la toxicologie animale.
MedDRA est actuellement disponible dans 14 langues : Chinois, Tchèque, Néerlandais, Anglais, Français, Allemand, Hongrois, Italien, Japonais, Portugais, Espagnol, Russe, Coréen Et Portugais Brésilien.
Le domaine d’application du MedDRA comprend :
- Signes/ symptômes.
- Indications thérapeutiques – dont les signes, symptômes, maladies, diagnostics ou prophylaxie d’une maladie et modification d’une fonction physiologique.
- Noms et résultats qualitatifs des investigations.
- Termes se rapportant aux erreurs médicamenteuses et aux problèmes de qualité d’un produit.
- Interventions chirurgicales et médicales.
- Antécédents médicaux, sociaux, familiaux.
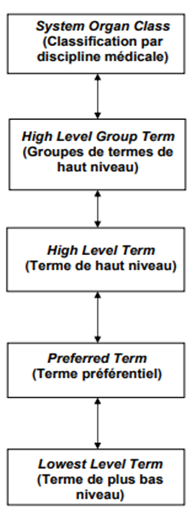
La hiérarchie MedDRA est composée de cinq niveaux :
- LLT : niveau le plus spécifique, termes qui se rapprochent le plus de la manière dont les informations sont rapportées.
- PT : descripteur distinct (concept médical unique) pour un symptôme, un signe, un diagnostic de maladie, une indication thérapeutique, une investigation, une intervention chirurgicale ou médicale et une caractéristique médicale, sociale ou familiale.
- HLT : groupe de PT apparentés basés sur l’anatomie, la pathologie, la physiologie, l’étiologie ou la fonction.
- HLGT : groupe de HLT apparentés basés sur l’anatomie, la pathologie, la physiologie, l’étiologie ou la fonction.
- SOC : niveau de classification le plus large groupant les termes selon l’une des trois catégories :
- Par système anatomique ou physiologique (g. : SOC Affections cardiaques).
- Par étiologie (g. : SOC Infections et infestations).
- Par but/ finalité (g. : SOC Actes médicaux et chirurgicaux).
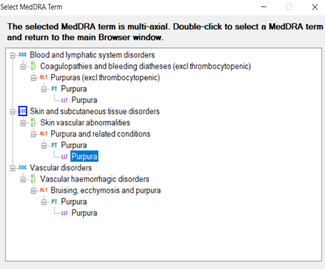
Chaque terme MedDRA se voit attribuer un code numérique à 8 chiffres, e.g.: Purpura= 10037549, ce code est unique quel que soit la langue utilisée.
La hiérarchie MedDRA peut être multiaxiale, ce qui signifie qu’un PT peut exister dans plusieurs SOC.
Il existe deux versions par an :
- Version complexe en mars XX.0: les changements concernent toute la hiérarchie MedDRA (SOC, HLGT,HLT,PT,LLT).
- Version simple XX.1 septembre: les modifications concernent uniquement les niveaux PT et LLT.
La dernière version de MedDRA est la 25.0 en mars 2022 composée de :
| PT | LLT | HLT | HLGT | SOC | |
| Version 25.0 | 85091 | 25412 | 1737 | 337 | 27 |
Des recommandations de codage afin d’assurer un codage correct et cohérent avec la dernière version de MedDRA en vigueur publiée, sont disponibles dans un document édité par le MSSO à chaque version complexe du MedDRA : MedDRA term selection – Points to Consider.
L’une des recommandations :
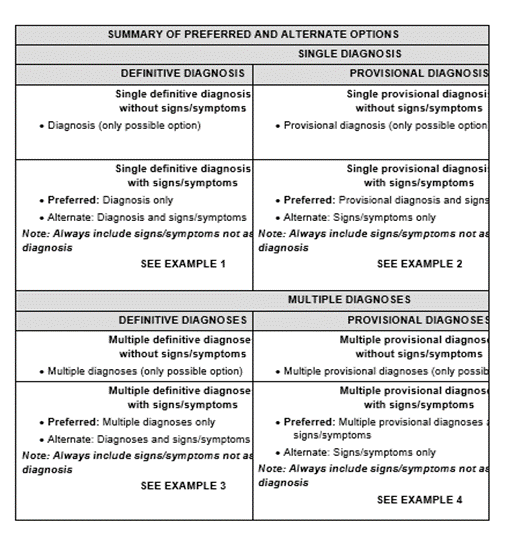
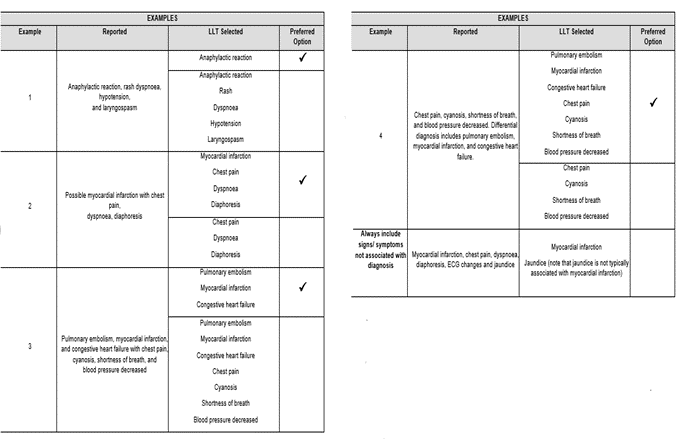
Le MedDRA nous offre la possibilité de réaliser une extraction des cas individuels qui sont potentiellement pertinents pour l’affection ou le domaine d’intérêt étudié par des listes (plus de 200 listes) prédéfinies composées de PTs. Il s’agit des QUESTIONS MedDRA NORMALISÉES : SMQ (STANDARDISED MedDRA QUERY).
Chaque SMQ est composée, par rapport au domaine d’intérêt étudié, d’un ensemble de termes :
- Très spécifiques (narrow scope) : en bleu.
- Moins spécifiques (broad scope) : en rouge.
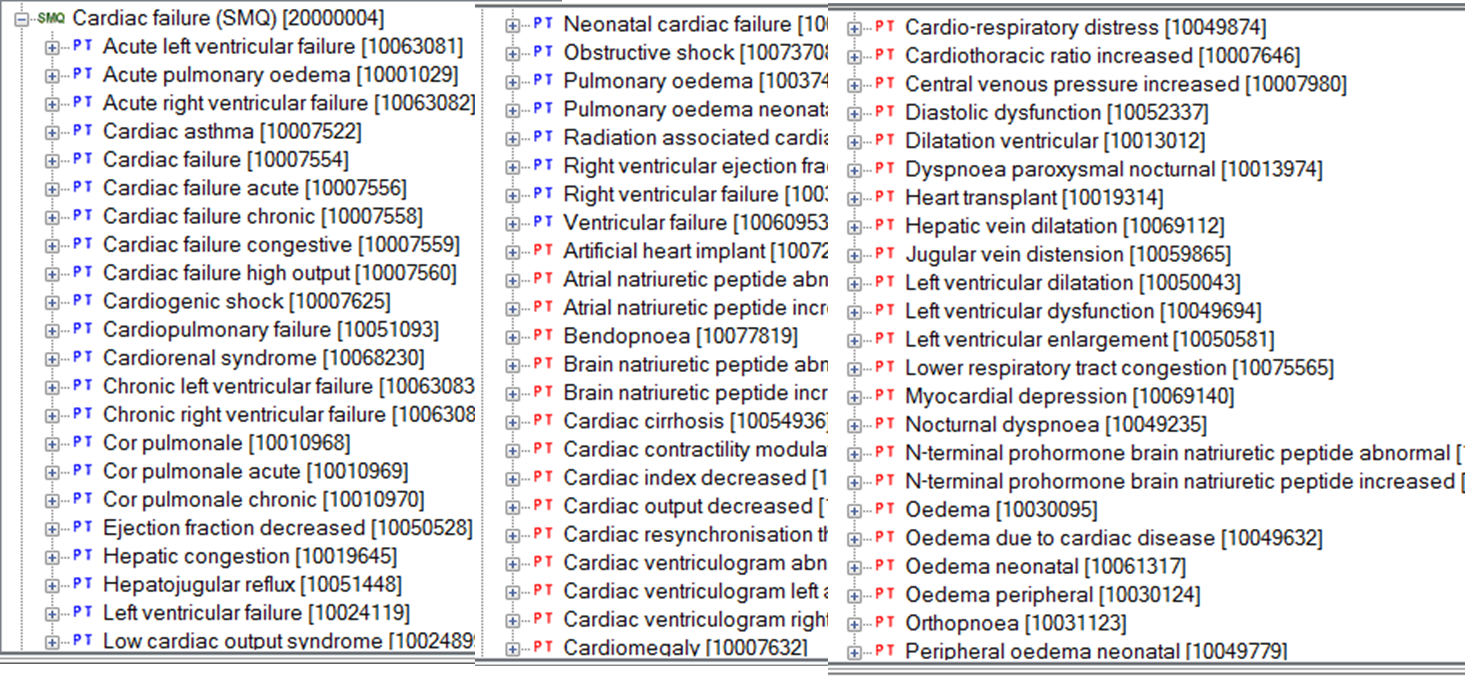
La règle d’or pour assurer un bon usage du MedDRA : plus les données rapportées sont précises, plus le codage sera précis et meilleure et minutieuse sera notre analyse des données.